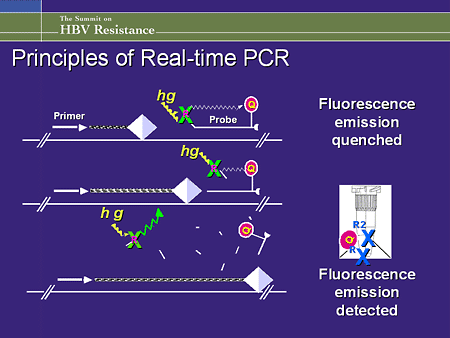
Real-time PCR
این
تکنیک کاربردهای وسیعی در تشخیص بالینی و تحقیقات دارد. در این روش میتوان
یک سکانس خاص را در DNAی هدف، جستجو و شناسایی کرد و همچنین مقدار آن را
در نمونهای مورد مطالعه اندازه گیری نمود. در این تکنیک نیز اصول کلی PCR
حاکم است ولی نکته حائز اهمیت این است که پس از تکثیر DNA در هر سیکل، غلظت
دقیق آن اندازه گیری میشود. سایر نامهای این تکنیک عبارتند از
quantitative real time polymerase chain
reaction و kinetic polymerase chain reaction. این تکنیک گاهی به اشتباه
RT-PCR نامیده میشود که مخفف روش Reverse Transcription PCR است. ولی
امروزه در دنیای تجارت و حتی مراکز تحقیقاتی بصورت یک اشتباه مصطلح در آمده
است. گاهی روش Real-time PCR با رونویسی معکوس(reverse transcription)
ادغام میگردد تا مقدار mRNA (messenger RNA) در سلولها و بافتها اندازه
گیری شود. این تکنیک جدید، Real-time reverse-transcription PCR نامیده
میشود و با علامتهای اختصاری qRT-PCR، RRT-PCRو یا RT-rt PCR مشخص میگردد.
در تکنیک Real-time PCR، برای تعیین غلظت DNA از رنگهای فلورسانس و یا شاخص های الیگونوکلئوتیدی فلورسانس استفاده میشود.
تعیین غلظت DNA با استفاده از رنگهای فلورسانس
در
این تکنیک از رنگهایی استفاده میشود که پس از اتصال به ساختار دو رشته ای
DNA (double-stranded:ds)، نور فلورسانس منتشر میکنند. بنابر این در طی
واکنش PCR، به موازات افزایش غلظت DNA، میزان فلورسانس در محلول افزایش می
یابد. با اندازه گیری شدت نور فلورسانس در انتهای هر سیکل، نهایتا یک منحنی
بدست می آید. سپس با استفاده از نمودارهای استاندارد، غلظت DNAی هدف در
نمونه مورد مطالعه محاسبه میشود. لازم به ذکر است که رنگهایی نظیر SYBR
Green به تمام انواع DNAی دو رشته ای، ازجمله محصولات غیر اختصاصی PCR و
حتی دیمرهای پرایمر (Primer dimers) نیز متصل میشوند و این موضوع موجب کاهش
اختصاصی بودن (Specificity) در نتایج حاصل میشود.
تعیین غلظت DNA با استفاده از شاخص های الیگونوکلئوتیدی فلورسانس
در
تکنیک Real-time PCR، دقیقترین و قابل اعتمادترین نتایج با استفاده از
شاخص های گزارشگر فلورسانس بدست می آید که البته هزینه زیادی نیز در
بردارد. در این روش از شاخصهای DNA یا RNA ی اختصاصی (sequence-specific
RNA or DNA-based probe) استفاده میشود و در نتیجه در DNAی هدف، جستجو و
تعیین غلظت برای سکانسهای خاص امکانپذیر میگردد. بنابر این حتی در حضور
سایر انواع DNA، نتایج حاصل از نظر اختصاصی بودن، در حد بالائی است. در این
شرایط، چنانچه از شاخصهای اختصاصی با رنگهای مختلف استفاده شود، حتی
میتوان ژنهای متعددی را در یک واکنش PCR، مورد بررسی قرار داد.
کاربردهای Real-time PCR:
1. تعیین تعداد کپی از هر ژن: Wu, 2007; ABI TaqMan® Gene Copy Number Assays; Protocol for 7900HT
2. سنجش میزان بیان ژن:Giulietti, 2001 و Leung, 2005
3. بررسی صحت نتایج در آرایه ها: Rajeevan, 2001 و Verification of Array Results Page by Pfaffl
4. مطالعات ایمنی زیستی و پایداری ژنتیک: Lovatt, 2002
5. بررسی میزان اثر بخشی داروها و مانیتورینگ داروها: Leruez-Ville, 2004; Brennan, 2003; Burger, 2003; Kogure, 2004
6. انجام تکنیک Real-Time Immuno-PCR (IPCR): Adler, 2003; Barletta, 2004; Lind & Kubista, 2005
7.
رسوب کروماتین با استفاده از اتصال آنتی ژن-آنتی بادی: Braveman, 2004;
Sandoval, 2004; Wang, 2004; Iype, 2005; Potratz, 2005; Puppo, 2005
8. سنجش ویروسها: Niesters, 2001; Mengelle, 2003; Espy, 2006
9. شناسائی عوامل پاتوژن شامل:
شناسائی CMV: Kearns, 2001a; Kearns, 2001b; Kearns, 2002; Mengelle, 2003
تشخیص سریع آلودگی به مننگوکوک: Bryant, 2004
بررسی حساسیت استرپتوکوکوس پنومونیا به پنی سیلین : Kearns, 2002
شناسائی مایکوباکتریوم توبرکولوزیس و گونه های مقاوم: Kraus, 2001; Torres, 2003; Cleary, 2003; Hazbon, 2004
پاتوژن های میکروبی در آبهای محیطی: Foulds, 2002; Guy, 2003
10. اندازه گیری میزان آسیب به DNA: Dietmaier, 2001
11. سنجش میزان تماس با اشعه رادیواکتیو: Blakely, 2001; Blakely, 2002; Grace, 2002; Grace, 2003
12. بررسی فرآیندهای زیستی در سلولهای زنده: Tung, 2000; Bremer, 2002
13. مطالعه DNAی میتوکندریائی: He, 2002; Liu, 2003; Alonso, 2004
14. شناسائی متیلاسیون: Trinh, 2001; Cottrell, 2004; Lehmann & Kreipe, 2004; Thomassin, 2004
15. تشخیص غیرفعال شدن ژنها در کروموزوم X: Hartshorn, 2002; van Dijk, 2002
16. تعیین همسانی در لوکوسهای HLA: Zhou, 2004
17. پیگیری نتایج پیوند عضو: Sabek, 2002; Gibbs, 2003
18. پیگیری نتایج، پس از پیوند سلولهای بنیادی خونساز: Elmaagacli, 2002; Alizadeh, 2002; Thiede, 2004; Harries, 2004
19.
پیگیری عوارض باقیمانده ناشی از بیماری، پس از پیوند سلولهای بنیادی
خونساز: Elmaagacli, 2002; Cilloni, 2002; Sarris, 2002; Gabert, 2003; Van
der Velden, 2003
20. تعیین مقدار ژن و زیگوسیتی: (Bubner, 2004; Barrois, 2004; Chen, 2006; Szilagyi, 2006
21.
ژنوتایپینگ و تشخیص انواع موتاسیونها شامل الحاق، حذف و موتاسیون نقطه ای:
von Ahsen 2000; Donohoe, 2000; Lyon, 2001; Waterfall & Cobb, 2002;
Bennett, 2003; Wittwer, 2003; Zhou, 2005; Palais, 2005; Chou, 2005، ;
Mhlanga, 2001; Solinas, 2001; Song, 2002; Gupta, 2004; reviewed in
Lareu, 2004، Kutyavin, 2000; Letertre, 2003; Johnson, 2004; Ugozzoli,
2004، Tapp, 2000
22. بررسی انواع تریزومی: Zimmermann, 2002
23. بررسی ژنوتیپهای حاصل از حذف جزئی یا microdeletion: Laurendeau, 1999; Kariyazono, 2001; Covault, 2003; Coupry, 2004
24. هاپلوتایپینگ: Von Ahsen, 2004; Pont-Kingdon & Lyon, 2005
25. بررسی کمی میکروساتلیت ها: Ginzinger, 2000
26.
تشخیص قبل از تولد و تعیین جنسیت با استفاده از سلولهای جدا شده از خون
مادرHahn, 2000; Bischoff, 2002; Bischoff, 2003 یا DNAی جنینی در جریان
خون مادر Bischoff, 2002; Hwa, 2004
27. تشخیص قبل از تولد برای اختلالات هموگلوبین: Kanavakis, 1997; Vrettou, 2003; Vrettou, 2004
28. تشخیص سرطان در حین عمل جراحی : Raja, 2002
LATE-PCR که یک نوع real-time PCR جدید است و بررسی های کمی را در مقادیر
جزئی از نمونه های بیولوژیک، امکانپذیر میسازد و بتریج کاربردهای وسیعی در
تشخیص بالینی، دفاع بیولوژیک، پزشکی قانونی و تعیین سکانس DNA می یابد.
برگرفته از : ژنتیک پزشکی
